25 种佐剂 “基因指纹” 公开!这个数据库让疫苗开发效率翻倍
应用介绍
,这是首个整合 25 种核心疫苗佐剂转录组数据与血液、生化 metadata 的多物种资源平台。该数据库通过标准化实验方案,实现了与毒理基因组学数据库 Open TG-GATEs(OTG)的跨库整合,借助机器学习模型成功预测了佐剂的ADB 的建立为疫苗佐剂的高效筛选、作用机制解析及生物标志物发现提供了标准化平台,推动了系统疫苗学在新型疫苗与免疫疗法开发中的应用,对提升疫苗安全性与有效性具有重要意义。

疫苗佐剂是疫苗配方中增强免疫应答的关键成分,不仅能提升疫苗对传染病的预防效果,还在癌症免疫疗法等领域展现出治疗潜力。然而,佐剂的疗效与安全性评估长期面临挑战:现有方法存在生物可变性大、实验条件不一致等问题,导致筛选效率低、结果可重复性差。
以新冠疫情为例,mRNA 疫苗、灭活疫苗等多种技术路线的成功应用均依赖于佐剂的优化 —— 如 mRNA 疫苗中的脂质纳米粒(LNP)作为内源性佐剂,可有效激活先天免疫。但佐剂的 “双刃剑” 效应显著:部分佐剂可能引发过度炎症或器官毒性,如完全弗氏佐剂(CFA)因强炎症反应仅能用于实验研究。因此,系统化、高通量的佐剂评估工具成为疫苗开发的迫切需求。
ADB 的构建基于与 Open TG-GATEs(OTG)一致的标准化实验方案,后者是已广泛应用的毒理基因组学数据库,涵盖 150 种化合物的毒性数据。这种设计确保了两者的兼容性,为同时预测佐剂性与毒性奠定基础。
数据类型:基因表达谱(Affymetrix 基因芯片)、血液学指标(如白细胞计数)、血清生化指标(如 ALT,肝损伤标志物)及组织病理学结果。
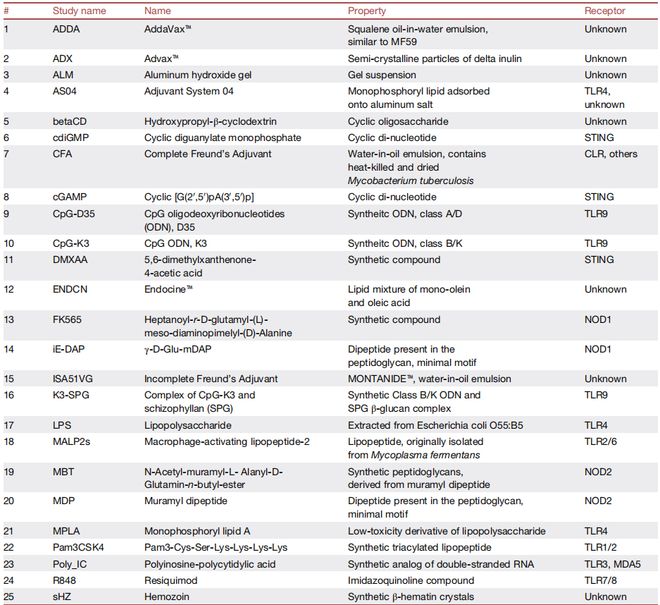
新型候选佐剂:如环二核苷酸(cGAMP,STING 激动剂)、β- 环糊精(betaCD,诱导损伤相关分子释放)。表 1 列出了 ADB 中的核心佐剂及其作用靶点
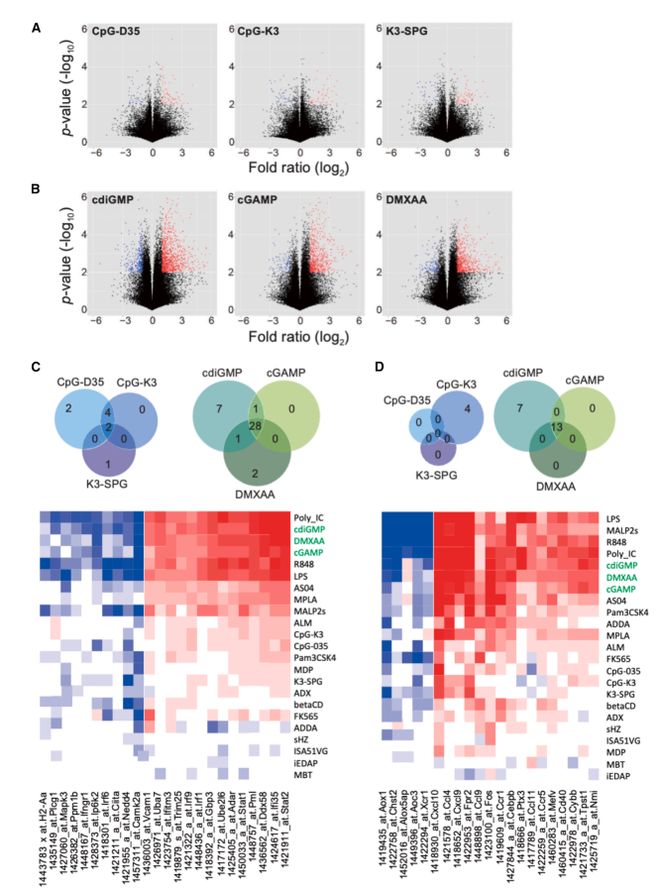
通过层级聚类分析和主成分分析(PCA),研究发现每种佐剂在不同器官和物种中均呈现独特的基因表达 “指纹”。例如,核酸类佐剂(如 Poly_IC、cGAMP)在小鼠的脾脏、肝脏和淋巴结中始终聚类在一起,而 LPS 与它的低毒衍生物 MPLA 则因炎症基因激活强度不同而明显分离(图 1A、1B)。这一发现表明,基因表达谱可作为区分佐剂类型及作用机制的分子标志物。
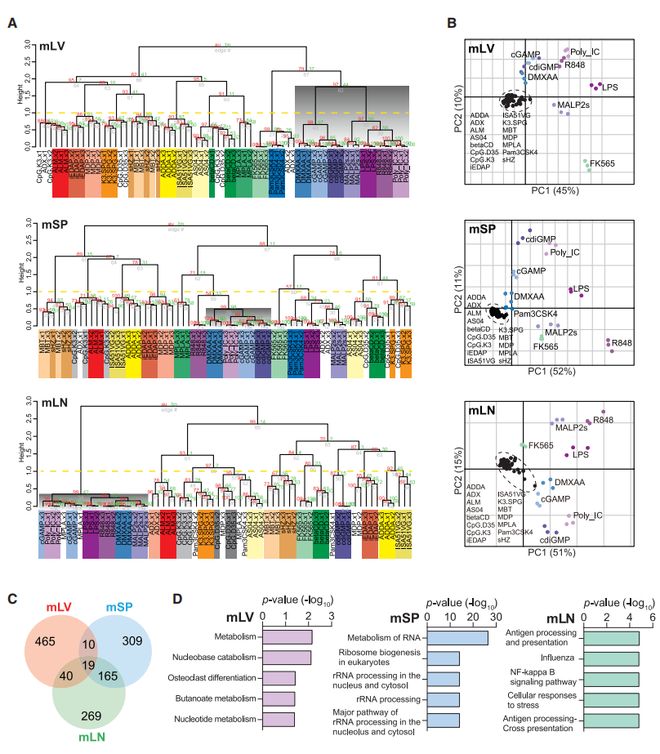
(A)层级聚类显示核酸类佐剂在不同器官中聚类(阴影部分);(B)PCA 显示佐剂在基因表达模式上的显著分离
ADB 数据揭示了佐剂诱导的炎症反应与干扰素通路激活的时间动态。例如,CpG ODN 和 AS04 在 24 小时时上调干扰素相关基因,表明其免疫激活存在延迟效应;而 MALP2s、FK565 则在 6 小时内显著诱导急性炎症基因(如 A2m)的表达(图 S2)。此外,血液学数据显示,多数佐剂会引发淋巴细胞减少,且这种变化与肝脏、脾脏中的特定基因表达高度相关(r0.9),提示全身免疫激活与局部基因调控的关联(图 2)。
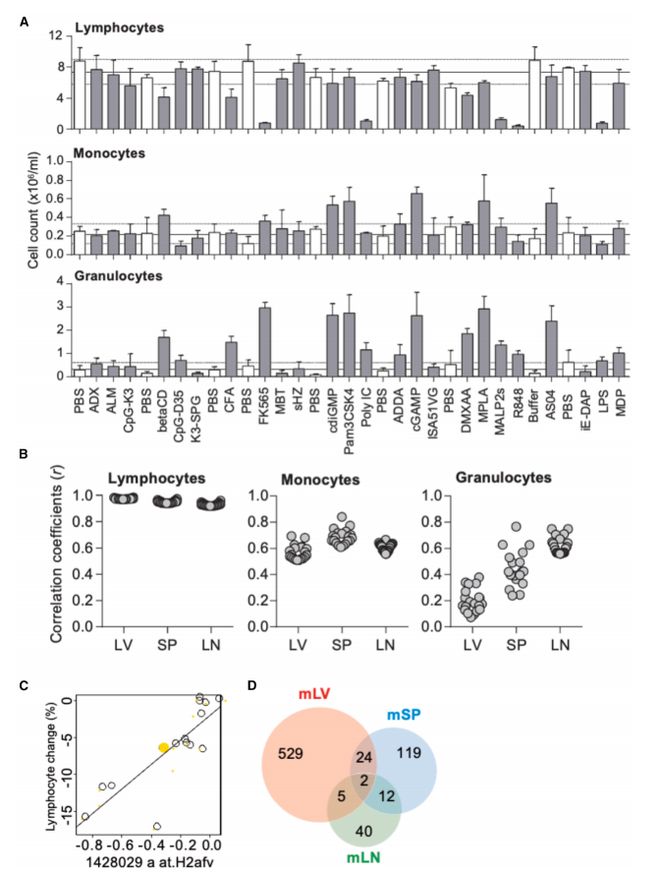
(A)佐剂诱导的淋巴细胞、单核细胞和粒细胞数量变化;(B)血液细胞计数与器官转录组的相关性热图
利用 OTG 中 150 种化合物的大鼠肝脏转录组数据(21 种有毒性,24 种无毒性),研究构建了基于支持向量机(SVM)的肝坏死预测模型。将该模型应用于 ADB 中的佐剂,发现 NOD1 激动剂 FK565 被预测为高肝毒性。实验验证显示,FK565 给药后 24 小时,大鼠血清 ALT(肝损伤标志物)显著升高,且小鼠肝脏出现病理损伤(图 4C、4E),同时伴随脂质代谢紊乱和凝血功能异常(图 4D)。
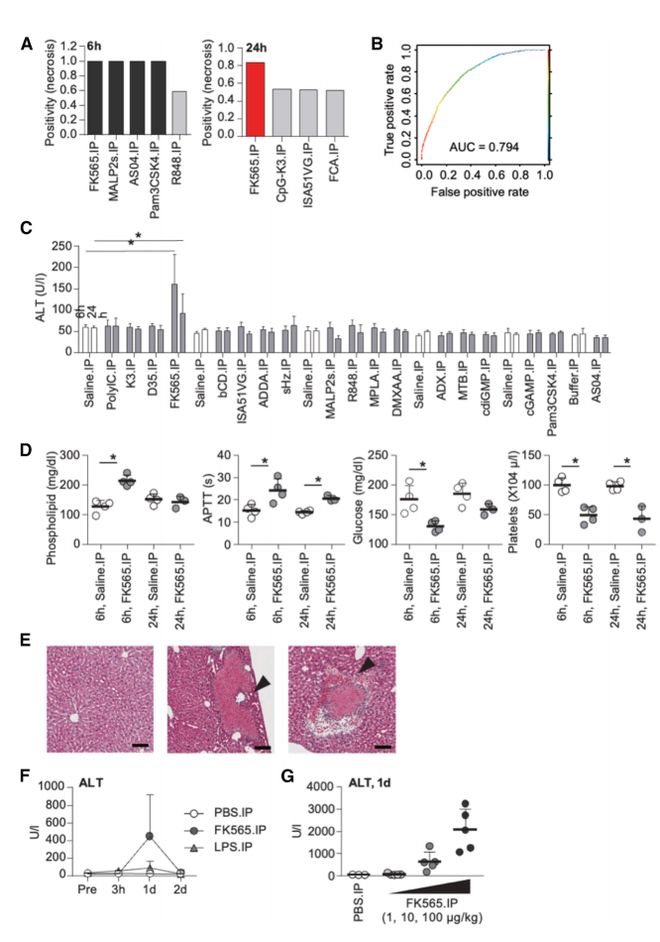
(C)FK565 显著升高大鼠血清 ALT 水平;(E)小鼠肝脏组织切片显示 FK565 诱导的损伤(箭头所示)
以 ADB 中 3 种安全有效的佐剂(ALM、ADDA、ISA51VG)为阳性对照,OTG 中 23 种无免疫激活作用的化合物为阴性对照,构建的佐剂性预测模型成功从 OTG 中筛选出潜在佐剂。其中,秋水仙碱(colchicine,传统抗痛风药物)被预测具有强佐剂性。实验证实,秋水仙碱与卵清蛋白(OVA)共注射可诱导高水平 OVA 特异性 IgG 抗体,并激活 CD8⁺ T 细胞(IFN-γ)和 Th2 型细胞因子(IL-5),表明其能同时诱导先天和适应性免疫应答(图 6D、6E)。
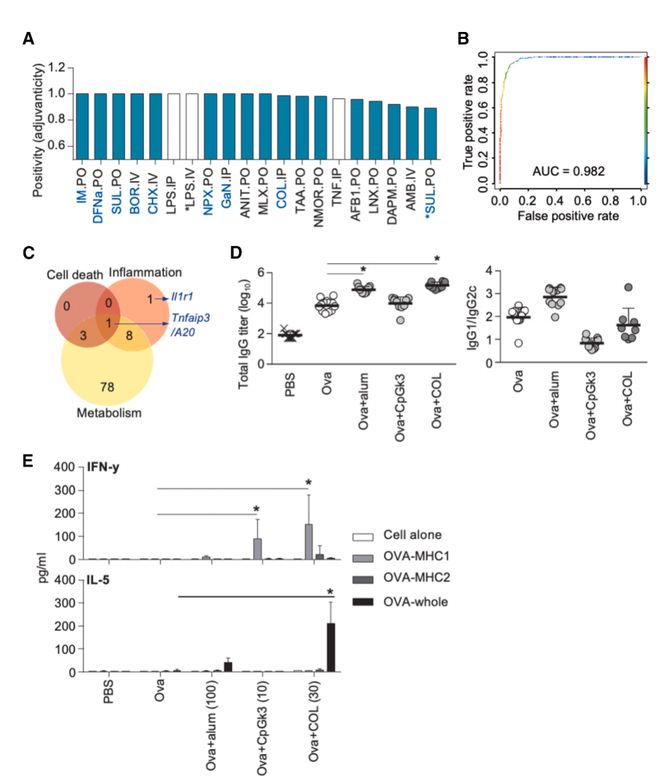
(D)秋水仙碱诱导的 OVA 特异性 IgG 抗体滴度;(E)脾细胞中 IFN-γ(Th1)和 IL-5(Th2)的分泌水平
ADB 数据揭示了同一家族佐剂的功能差异。例如,TLR9 激动剂 CpG-D35 与 CpG-K3 虽均靶向 TLR9,但前者主要激活干扰素通路(早期内体定位),后者则强诱导炎症反应(晚期内体定位)(图 3A、3C)。这种差异为精准设计佐剂、调控免疫应答类型(如 Th1/Th2 偏向)提供了依据。
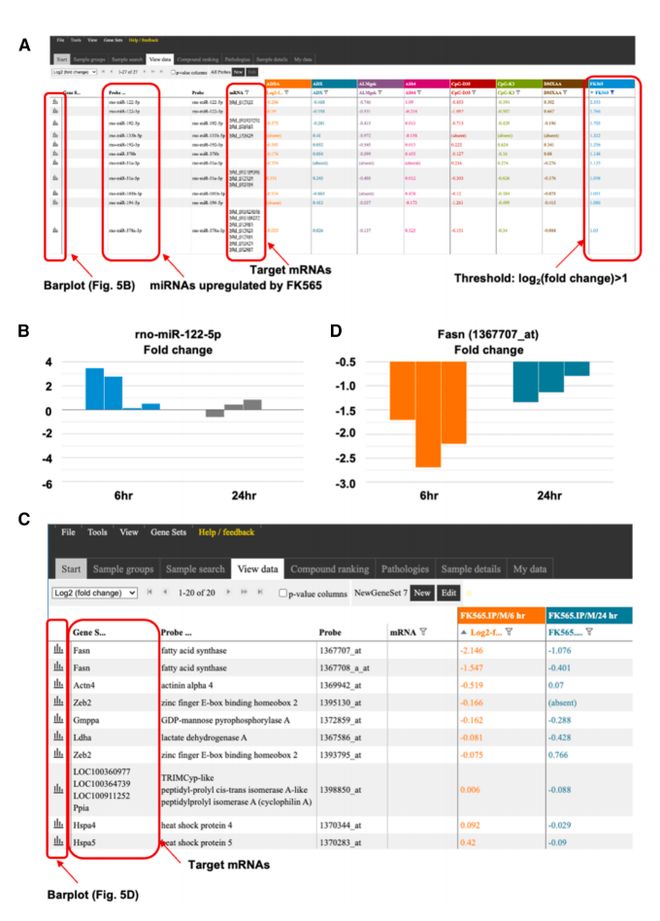
ADB 的 miRNA 数据显示,FK565 诱导的肝损伤伴随血清中 miR-122-5p 显著升高(log2 倍变化 = 2.35),其靶基因 Fasn(脂肪酸合成酶)表达下调(图 5)。这一发现与已知 miR-122 作为肝损伤标志物的研究一致,表明 ADB 可用于筛选新型无创性毒性 biomarkers。
数据驱动发现:机器学习模型与实验验证的闭环,加速了新型佐剂的挖掘(如秋水仙碱)和风险预警(如 FK565)。
未来,ADB 将进一步整合人类临床数据(如疫苗接种者的血液样本),并拓展至更多物种(如非人灵长类),以提升从临床前到临床转化的准确性。此外,与国际疫苗佐剂联盟(如 ENOVA)的数据融合,有望构建全球协作的佐剂评估网络。
当前 ADB 的主要局限在于缺乏人类转录组数据,这受限于健康志愿者单独接种佐剂的伦理约束。未来需通过疫苗临床试验中的佐剂 - 抗原联合数据间接分析,或开发类器官模型替代动物实验,以填补这一空白。